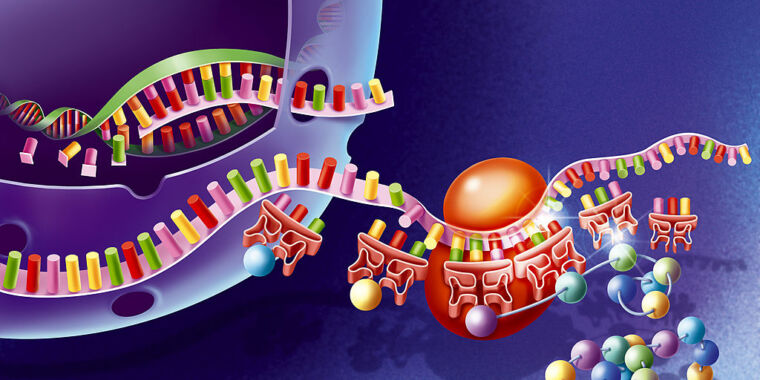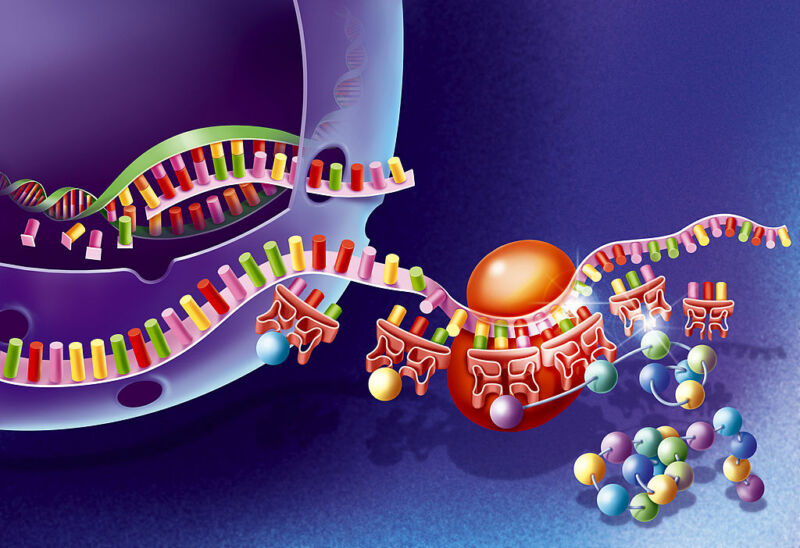
تستخدم جميع الكائنات الحية على الأرض نفس الإصدار من الشفرة الجينية. كل خلية تصنع البروتينات باستخدام نفس الأحماض الأمينية العشرين. تقرأ الريبوسومات ، وهي الآلات التي تصنع البروتينات داخل الخلايا ، الشفرة الجينية من جزيء الحمض النووي الريبي المرسال لمعرفة الأحماض الأمينية التي يجب وضعها بجوار البروتين المحدد الذي تصنعه.
هذا الرمز عالمي ، ولهذا السبب يمكن للريبوسومات في خلايانا قراءة جزء من الحمض النووي الريبي المرسال الفيروسي وإخراج بروتين فيروسي وظيفي منه. هناك الكثير من الأحماض الأمينية الأخرى. على الرغم من أن الحياة لا تستخدمها عادة ، إلا أن العلماء يدمجونها في البروتينات. الآن ، وجد الباحثون طريقة لتوسيع الشفرة الجينية بشكل كبير ، مما يسمح بدمج هذه الأحماض الأمينية غير البيولوجية على نطاق واسع. لقد حققوا ذلك عن طريق تنشيط مجموعة ثانية من البروتينات والحمض النووي الريبي اللازمين لترجمة الشفرة الجينية.
باستثناء نظام واحد
يمكن للأحماض الأمينية الكنسية أداء العديد من الوظائف. يمكن أن تكون بمثابة ملصقات بحيث يمكن بسهولة تتبع البروتين ذي الأهمية الخاصة للباحث داخل الخلايا. يمكن أن تساعد في تنظيم نشاط البروتين ، مما يسمح للباحثين بتنشيطه وإلغاء تنشيطه في وقت ومكان محددين من اختيارهم ، ثم مراقبة التأثيرات النهائية. عندما يتم الجمع بين هذه الأحماض الأمينية الاسمية معًا بكميات كافية ، فإن البروتينات الناتجة تشكل أنواعًا جديدة تمامًا من البوليمرات الحيوية التي يمكنها أداء وظائف لا تستطيع البروتينات التقليدية القيام بها – للبحث أو العلاج أو لأغراض أخرى.
لوضع الأحماض الأمينية غير الكنسية في البروتينات ، يجب تقليل الكود الجيني بحيث لا توجد طريقة لتحديد استخدامها. خيار قم بتحرير الشفرة الجينية للخلية، يترك معظمها سليمة. يستخدم نسخًا معدلة من جميع مكونات الشفرة الوراثية البديلة: mRNAs المتعامدة ، والريبوزومات المتعامدة والإنزيمات المتعامدة المسؤولة عن دراسة mRNAs وبناء البروتينات داخل الريبوسومات. المتعامد يعني أن هذه الآلة تعمل جنبًا إلى جنب مع آلة عادية لإنتاج بروتين الريبوسوم في الخلية ولكنها لا تتداخل معها. يقرأ ويترجم فقط MRNAs المتعامدة الخاصة به ، وليس الخلايا الخلوية العادية.
هذه العناصر المتعامدة خارجية ، وبالتالي فهي ليست ضرورية لوظيفة الخلية. لذلك يمكن تصميمها وترتيبها بشكل مختلف وتعديلها بطريقة يحلم بها العلماء. يمكن استخدامها لإنشاء بوليمرات جديدة وإلقاء الضوء على الآليات المشاركة في إنتاج البروتين الخلوي الطبيعي. هذا شيء لا يمكننا فعله بالمكونات الخلوية العادية لأنه يقتل الخلية.
تحسين التعامد
جايسون تشين، كامبردج ، رئيس مركز المواد الكيميائية والبيولوجيا التركيبية في المملكة المتحدة لكنها ليست فعالة للغاية. في ورقة نشرت هذا الأسبوع كيمياء طبيعيةيصف كيف قام بإصلاحها: يمكنه تلقائيًا تصميم وتحسين أي من الرنا المرسال المتعامد يتم ترجمته بشكل أفضل عن طريق الريبوسومات المتعامدة باستخدام الأساليب الحسابية. لم يحسن إنتاجية البروتين بشكل كبير فحسب ، بل أكد أيضًا أن الريبوسومات المتعامدة تعمل بشكل فعال حتى عندما تكون الطفرات ريبوسومات طبيعية.
تندب مقدمة العمل أن “فهمنا للعوامل التي تحدد إنتاجية البروتين للترجمة الطبيعية غير مكتمل … فقط نصف الاختلافات في إنتاجية البروتين المرصودة يمكن تفسيرها من خلال معلمات معروفة”. ومع ذلك ، علم مختبره أن الإجراء الأولي كان خطوة مهمة في التقاط الحمض النووي الريبي المرسال. لقد عرفوا أيضًا أن بنية MRNA كانت مهمة. لذلك بدأوا في تعديل mRNA المتعامد لتغيير هاتين الميزتين واختاروا تلك الطفرات التي تربط الريبوسومات المتعامدة جيدًا ولكن تحتوي على عدد أقل من الريبوسومات العادية. بعد مئات الجولات من الطفرات ، قاموا بتحسين ثلاثة أنواع مختلفة من MRNAs المتعامدة وقاموا بترميز ثلاثة بروتينات مختلفة. يحتوي أحدهم على أربعة أحماض أمينية اسمية.
استخدم المختبر في وقت لاحق نفس النهج لتحسين الإنزيمات المتعامدة ، وأنتجوا زيادة قدرها 33 ضعفًا في محصول البروتين ؛ ينتج النظام المتعامد الآن البروتين تمامًا مثل النظام الخلوي العادي. الخلايا المستخدمة في هذا العمل ه – حارس المرمى، لكن د. سين خميرة استخدمت طريقة متعامدة لإنتاج بروتينات غير متعارف عليها في خلايا الثدييات والديدان وذباب الفاكهة.
كتب هو وزملاؤه: “نتوقع أن يزداد عدد الأحماض الأمينية الفريدة غير المحددة مع زيادة فرص الخروج من مناهج الجمع بين العديد من الأحماض غير الكنسية الفريدة”. هذه الخوارزميات التي طوروها لتصميم MRNAs المتعامد المترجمة بشكل فعال ستساعد بالتأكيد على التحرك نحو هذا الهدف.
كيمياء طبيعية 2021. DOI: 10.1038 / s41557-021-00764-5

“متعصب للموسيقى. مستكشف متواضع جدا. محلل. متعصب للسفر. مدرس تلفزيوني متطرف. لاعب.”