
قدم باحثو جامعة كاليفورنيا في سان دييغو خلية متكاملة متعددة المقاييس (MuSIC) ، وهي تقنية تدمج الفحص المجهري والكيمياء الحيوية والذكاء الاصطناعي ، وتكشف عن مكونات خلوية غير معروفة سابقًا يمكن أن توفر أدلة جديدة على التطور البشري والمرض. (العرض الأيديولوجي للفنان.) الائتمان: جامعة كاليفورنيا في سان دييغو للعلوم الصحية
تكشف التقنية القائمة على الذكاء الاصطناعي عن مكونات خلوية غير معروفة سابقًا يمكن أن توفر أدلة جديدة للتطور البشري والمرض.
يمكن لمعظم الأمراض التي تصيب الإنسان اكتشاف الأجزاء المختلة وظيفيًا في الخلية – فالورم قادر على النمو لأن الجين لا يُترجم بدقة إلى بروتين معين ، أو أن الميتوكوندريا لا تحترق بشكل صحيح ، مما يسبب مرضًا استقلابيًا ، على سبيل المثال. ولكن لفهم أجزاء الخلية التي تصاب بمرض ما ، يجب أن يكون لدى العلماء أولاً قائمة كاملة بالمكونات.
من خلال الجمع بين الفحص المجهري وتقنيات الكيمياء الحيوية والذكاء الاصطناعي ، حقق الباحثون والمتعاونون في جامعة كاليفورنيا ، كلية الطب في سان دييغو ما يعتقدون أنه يمكن أن يكون اختراقًا مهمًا في فهم الخلايا البشرية.
تم وصف هذه التقنية ، التي تسمى الخلية المتكاملة متعددة النطاقات (MuSIC) ، في 24 نوفمبر 2021. طبيعي >> صفة.
قال أستاذ في جامعة كاليفورنيا سان دييغو: “إذا تخيلت خلية ، فمن المحتمل أنك رسمت خريطة ملونة بالميتوكوندريا ، والشبكة الإندوبلازمية والنواة في كتاب بيولوجيا الخلية. ولكن هل هذه هي القصة بأكملها؟ بالطبع لا”. الطب والدكتوراه “لقد أدرك العلماء منذ فترة طويلة أننا لا نعرف أكثر مما نعرف ، ولكن الآن هناك طريقة أخيرًا للبحث بشكل أعمق.”
قادت إيما لوندبيرج من المعهد الملكي للتكنولوجيا KTH وجامعة ستانفورد في ستوكهولم بالسويد دراسة Ideker بدرجة الدكتوراه.
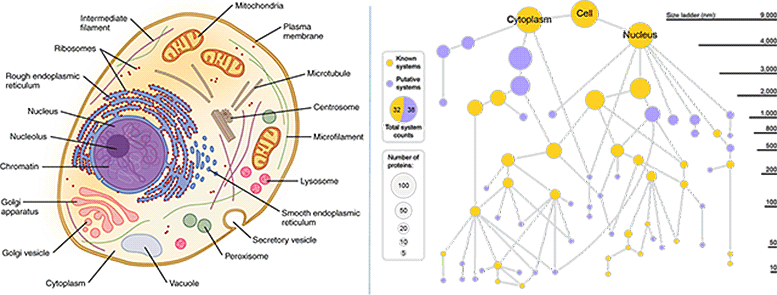
على اليسار: خرائط خلايا الكتب المدرسية التقليدية جميع المناطق مرئية ومحددة بوضوح. (الائتمان: OpenStocks / ويكيميديا). إلى اليمين: خريطة الخلية الجديدة التي تم إنشاؤها بواسطة تقنية MuSIC تكشف عن العديد من المكونات الجديدة. تمثل العقد الذهبية مكونات خلوية معروفة ، بينما تمثل العقد الأرجوانية مكونات جديدة. يعكس حجم العقدة عدد البروتينات الفريدة في تلك المكونات. الائتمان: العلوم الصحية بجامعة كاليفورنيا في سان دييغو
في الدراسة التجريبية ، كشف MuSIC عن حوالي 70 مكونًا في خط خلايا الكلى البشرية ، نصفها لم يسبق رؤيته من قبل. في أحد الأمثلة ، حدد الباحثون مجموعة من البروتينات التي تشكل هياكل غير مألوفة. من خلال العمل مع زميل جامعة كاليفورنيا في سان دييغو ، حاصل على درجة الدكتوراه ، جان يو ، حددوا في النهاية البنية المعقدة الجديدة لبروتينات الربط. RNA. قد يكون هذا المركب متورطًا في الانقسام ، وهي ظاهرة خلوية مهمة تساعد في ترجمة الجينات إلى بروتينات وتحديد الجينات التي يتم تنشيطها في أي وقت.
عادةً ما يتم فحص الأجزاء الداخلية للخلايا – والعديد من البروتينات الموجودة هناك – باستخدام إحدى طريقتين: التصوير المجهري أو الارتباط الفيزيائي الحيوي. من خلال التصوير ، يضيف الباحثون علامات فلورية بألوان مختلفة إلى البروتينات محل الاهتمام ويراقبون تحركاتها وتفاعلاتها تحت المجهر. لمعرفة التفاعلات الكيميائية الحيوية ، يستخدم الباحثون جسمًا مضادًا معينًا لبروتين ما لسحبه خارج الخلية ومعرفة ما يرتبط به أيضًا.
كان الفريق مهتمًا برسم خرائط الوظائف الداخلية للخلايا لسنوات عديدة. يختلف MuSIC من حيث أنه يستخدم التعلم المتعمق لتعيين الخلية مباشرة من صور المجهر الخلوي.
قال يو كين ، المؤلف الأول للدراسة ، وهو طالب دراسات عليا في المعلوماتية الحيوية وبيولوجيا الأنظمة في مختبر إديكر: “إن الجمع بين هذه التقنيات فريد وقوي لأنه تم تجميعها لأول مرة في مجموعة متنوعة من المقاييس”.
تسمح المجاهر للعلماء بقياس حجم ميكرون واحد حول حجم أعضاء معينة ، مثل الميتوكوندريا. لا يمكن رؤية المكونات الصغيرة مثل البروتينات الفردية ومجمعات البروتين من خلال المجهر. تسمح التقنيات الكيميائية الحيوية ، بدءًا من البروتين ، للعلماء بالنزول إلى مقياس النانومتر. (النانومتر هو جزء من جزء من المليار من المتر ، أو 1000 ميكرون).
“ولكن كيف تقلل هذه الفجوة من النانومتر إلى الميكرون؟ لقد كان هذا منذ فترة طويلة عقبة رئيسية في العلوم البيولوجية” ، هذا ما قالته ، مؤسس مبادرة خريطة خلية السرطان بجامعة كاليفورنيا ومؤسس مركز جامعة كاليفورنيا في سان دييغو للبيولوجيا الحاسوبية والمعلوماتية الحيوية. يمكن – إلقاء نظرة على البيانات من مصادر متعددة واطلب من الكمبيوتر دمجها في نموذج خلية. “
قام الفريق بتدريب منصة MuSIC للذكاء الاصطناعي على عرض جميع البيانات وإنشاء نموذج خلية. لم يقم الكمبيوتر بعد بتعيين محتويات الخلية لمواقع محددة ، مثل خريطة الكتاب المدرسي ، لأن مواقعها ليست ثابتة بشكل صارم. على العكس من ذلك ، تكون مواقع المكونات سائلة وتتغير حسب نوع الخلية والبيئة.
وأشار إيديكر إلى أن هذا اختبار تجريبي لاختبار MuSIC. لقد رأوا فقط 661 بروتينًا ونوعًا من الخلايا.
قال إيديكر: “المرحلة التالية الواضحة هي تفجير الخلية البشرية بأكملها”.
ملاحظة: يو كين ، إدوارد ل. هدلين ، كاسبار ف. فينيسيس ، مايا ل. كوستيلا ، لودوين فاتشول ، ماركوس ر. كيلي ، ستيفن م. Blu ، “خريطة فان متعددة الأبعاد لهياكل البروتين والتفاعلات التي تربط بنية الخلية” بقلم Zheng و Michael Chen و Lia V. شايفر ، كاثرين لاكون ، آنا باكستروم ، لورا بونتانو وايتس ، جون ج. لي ، وي أويانغ ، صوفي ن. ليو ، تيان تشانغ ، إيريكا سيلفا ، جيزو بارك ، أدريانا بيديا ، جايسون ف. جريس ستيفن بي جيجي ، جيانزو ما ، جيه ويد هاربر ، جين دبليو يو ، دينيس إل جيه لافونتين ، إيما لوندبرج وتري إيديكر ، 24 نوفمبر 2021 ، طبيعي >> صفة.
DOI: 10.1038 / s41586-021-04115-9
المؤلفون المشاركون: Maya L. كوستاريكا ، ماركوس ر. كيلي ، ستيفن م. بلو ، فان تشنغ ، مايكل تشين ، ليا ف. شايفر ، كاثرين ليغان ، جون ج. لي ، صوفي ن. ليو ، إيريكا سيلفا ، جيسو بارك ، أدريانا بيديا ، جايسون ف. كريسبرج ، جامعة كاليفورنيا في سان دييغو ؛ إدوارد ل. هودلين ، لورا بونتانو وايتس ، تيان زانج ، ستيفن ب. جيجي ، ج. ويد هاربر ، كلية الطب بجامعة هارفارد ؛ كاسبار ف. Vinceness، Anna Backstrom، Wei Oyang، KDH Royal Institute of Technology؛ Ludwine Vachul، Denise LJ Lafontaine، University Libre de Bruxels؛ وجيانزو ما ، جامعة بكين.
تم تمويل هذا البحث من قبل المعاهد الوطنية للصحة (تقدم U54CA209891 ، U01MH115747 ، F99CA264422 ، P41GM103504 ، R01HG009979 ، U24HG006673 ، U41HG009889 ، R01HL137223 ، R01HG004659 ، مؤسسة R50CA243885) والمشي ، ومشاة Google Ventures ، وجوجل Ventures (منحة 20160204) ، مجلس البحوث السويدي (منحة 2017-05327) ، الصناديق البلجيكية للبحوث العلمية ، جامعة Libre de Bruxels ، البرنامج الأوروبي المشترك للأمراض النادرة ، منطقة والون ، الدولية 1. CAST. )
الإفصاحات: Trey Ideker ، المؤسس المشارك للمجلس الاستشاري العلمي والمهتم بالمشاركة في Data4Cure، Inc. إيديكر هو أيضًا عضو في المجلس الاستشاري العلمي ، Ideaya BioSciences، Inc. يتلقى تمويل البحث من. جان يو هو مؤسس مشارك وعضو في مجلس الإدارة وشريك في المجلس الاستشاري العلمي ومستشار في الأجور لـ Locanabio و Eclipse BioInnovations. يو هو أيضًا أستاذ زائر في جامعة سنغافورة الوطنية. تمت مراجعة شروط هذه الترتيبات والموافقة عليها من قبل جامعة كاليفورنيا ، سان دييغو وفقًا لسياسة تضارب المصالح الخاصة بها. إيما لوندبرج عضو في المجلس الاستشاري العلمي وهي مهتمة بالمشاركة في علم الأحياء لرسم الخرائط ، التكنولوجيا الحيوية نوتيلوس وعلاجات إنترلاين. ج. ويد هاربر ، المؤسس المشارك للمجلس الاستشاري العلمي وهو مهتم بنفس القدر بعلاجات الكراوية. هاربر هو أيضًا مستشار علمي في Interline Therapeutics.

“متعصب للموسيقى. مستكشف متواضع جدا. محلل. متعصب للسفر. مدرس تلفزيوني متطرف. لاعب.”
